梅斯盘点:2022年妇瘤十大临床研究进展
妇瘤领域在2022年也获得不少进展,除乳腺癌外,卵巢癌,子宫内膜癌,宫颈癌都有不少新的临床研究突破,梅斯小编给您盘点一下今年的十大临床研究进展
1、DS-8201横空出世,让HER2+和HER2低表达乳腺癌患者获益
DS-8201是一个新型的ADC药物,由人源化抗HER2抗体+伊立替康类化疗药物的偶联药物组成。可裂解的连接子在血液循环中结构稳定,药物脱落率低,从而降低毒副反应,且DS-8201具有高效的“旁观者效应”。DS-8201目前在乳腺癌、胃癌、结直肠癌中进行了若干研究,显示出良好的抗肿瘤活性。
2022年6月5日,《新英格兰医学杂志》(NEJM)在线发表DESTINY-Breast04 研究结果。DESTINY-Breast04研究是一项全球、随机、开放标签3期临床试验,评估曲妥珠单抗-deruxtecan与医生选择的治疗方案(TPC)相比,在 HER2低表达、既往接受过解救治疗(HR阳性患者要求接受过内分泌解救治疗)的不可切除和/或转移性乳腺癌患者中的疗效和安全性。结果显著,引发全球学者的关注,见:NEJM:新型HER2-ADC Enhertu打破HER2低表达的乳腺癌治疗困境(DESTINY-Breast04)。随后FDA%27%3EFDA%3C/a%3E">FDA加速批准其上市,见:FDA提前4个月加速批准DS-8201治疗HER2低表达乳腺癌,超6成乳腺癌患者均能受益

2、T-DXd与T-DM1头对头对比中获胜
与T-DM1头对头对比中,又大获全胜。T-DXd治疗在无进展生存期方面比T-DM1有优势。T-DXd组的无进展生存期中位数未达到(95%CI,18.5至无法估计),T-DM1组为6.8个月(95%CI,5.6~8.2)。T-DXd组12个月后无进展生存率为75.8%,而T-DM1组为34.1%(全因死亡或疾病进展风险为0.28),详细见:Trastuzumab Deruxtecan治疗HER2阳性乳腺癌效果优于trastuzumab emtansine、Enhertu在DESTINY-Breast03中延长HER2阳性转移性乳腺癌统计学意义上总生存,比T-DM1降低死亡风险36%
3、帕博利珠单抗治疗晚期三阴性乳腺癌获得最终证据支持
在这项3期临床试验的中期分析中,在化疗中加入帕博利珠单抗(pembrolizumab,K药)比单独化疗治疗晚期三阴性乳腺癌患具有更长的无进展生存期,这些患者的肿瘤表达程序性死亡配体1(PD-L1)且联合阳性分数(CPS)为10或以上。最终结果显示在肿瘤表达PD-L1且CPS为10或更高的晚期三阴性乳腺癌患者中,相比单独化疗,在化疗中加入帕博利珠单抗带来了总生存期的明显延长。详细见:NEJM重磅:K药一线治疗三阴乳腺癌OS结果终现!,随后FDA也批准了K药的新适应症。
4、HR+乳腺癌取得系列进展
MONALEESA-2、MONALEESA-3以及MONALEESA-7研究的最新更新结果表明,瑞博西利联合内分泌治疗可为HR阳性、HER2阴性晚期乳腺癌患者带来统计学显著意义的PFS以及OS获益,同时还有相当多的新的研究结果。
(1)瑞博西利加来曲唑治疗晚期HR阳性乳腺癌的总体生存率
激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性疾病是转移性乳腺癌最常见的亚型,并且仍然无法治愈。在之前对该3期试验的分析中,在激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性的绝经后患者中,与单独采用来曲唑治疗相比,晚期乳腺癌采用一线瑞博西尼加来曲唑治疗的无进展生存期显著延长。不知道瑞博西尼的总生存期是否也会更长。研究人员报告了方案指定的总生存期最终分析结果,这是一个关键的次要终点。患者以1:1的比例随机分配接受瑞博西尼或安慰剂联合来曲唑。
中位随访6.6年后,瑞博西尼组334名患者(54.2%)发生181例死亡病例,安慰剂组334例(65.6%)患者发生219例死亡病例。与安慰剂加来曲唑相比,瑞博西尼加来曲唑具有显著的总体生存获益。瑞博西尼加来曲唑的中位总生存期为63.9个月(95%CI为52.4至71.0),安慰剂加来曲唑为51.4个月(95%CI为47.2至59.7)(死亡风险比为0.76;95%CI为0.63至0.93;两侧P=0.008)。没有观察到新的安全性事件。
由此可见,在HR阳性、HER2阴性晚期乳腺癌患者中,与安慰剂加来曲唑相比,瑞博西尼加来曲唑的一线治疗能具有显著的总体生存获益。瑞博西尼的中位总生存期比安慰剂长12个月以上。详细见:NEJM:瑞博西尼加来曲唑治疗晚期乳腺癌的总体生存率
(2)氟维司群联合Capivasertib治疗芳香化酶抑制剂耐药性晚期/复发性ER+HER2-乳腺癌
FAKTION研究是一项随机、多中心、双盲、安慰剂为对照的2期临床试验,招募了年满18岁、ER+HER2-、ECOG表现状态0-2分、经芳香化酶抑制剂治疗后进展或复发的转移性/局部晚期的不可手术的乳腺癌女性患者。受试患者被随机(1:1)分成两组,接受氟维司群+Capivasertib或安慰剂治疗直到病情进展、不可耐受的毒性、失访或撤出研究。主要终点是无进展生存期,次要终点包括总生存期和安全性。
2015年3月16日-2018年3月6日期间,筛查了183位患者,其中140位(77%)被随机分至氟维司群+Capivasertib组(n=69)或氟维司群+安慰剂组(n=71)。截止2021年11月25日,Capivasertib组和安慰剂组分别中位随访了58.5个月和62.3个月。Capivasertib组和安慰剂组的最新中位无进展生存期分别是10.3个月和4.8个月(校正风险比[HR] 0.56,p=0.0023)。Capivasertib组和安慰剂组的中位总生存期分别是29.3个月和23.4个月(校正HR 0.66,p=0.035)。FAKTION研究的最新数据显示,氟维司群加用Capivasertib可延长芳香化酶抑制剂耐药性ER+HER2-晚期乳腺癌患者的生存期。详细见:Lancet Oncol:氟维司群联合Capivasertib治疗芳香化酶抑制剂耐药性晚期/复发性ER+HER2-乳腺癌
(3)Abemaciclib联合内分泌治疗高风险早期乳腺癌
MonarchE研究旨在对比HR+HER2-高风险早期乳腺癌患者接受NAC±阿贝西利(Abemaciclib)治疗的疗效和安全性。这是一项多中心、开放标签的3期随机试验,招募了HR+HER2-淋巴结阳性、高复发风险的早期乳腺癌患者,随机(1:1)分成两组,予以标准的内分泌(ET)治疗至少5年,加用或不加用阿贝西利(150 mg,2次/日)治疗2年。主要终点是无侵袭性疾病生存率(IDFS)和无侵袭性疾病生存率(DRFS)。
2017年7月至2019年8月期间,共有2056位患者(平均49.9岁,2046位女性)进行了NAC治疗。截止2020年7月8日,中位随访了19个月。在亚组分析中,与单纯内分泌治疗相比,内分泌+阿贝西利治疗可明显改善患者的IDFS(HR 0.61)和DRFS(HR 0.61),相应的两年IDFS率和两年DRFS率分别绝对提高了6.6%和6.7%。而且,在病理乳腺肿瘤大小或阳性淋巴结数量的亚组中观察到了一致的治疗获益。
总之,阿贝西利联合内分泌辅助治疗可显著改善HR+HER2-、淋巴结阳性高复发风险早期乳腺癌患者的生存预后,包括无侵袭性疾病生存率和无侵袭性疾病生存率。详细见:JAMA Oncol:Abemaciclib联合内分泌治疗高风险早期乳腺癌
(4)新型高选择性CDK4/6抑制剂达尔西利可降低患者50%的疾病进展或死亡风险
DAWNA-1研究探索了达尔西利联合氟维司群治疗既往接受内分泌治疗后出现疾病进展的HR阳性、HER2阴性晚期乳腺癌的有效性及安全性,基于其中期分析的疗效,2021年12月获国家药品监督管理局批准上市。2022年ESMO大会更新了最新随访数据,达尔西利+氟维司群组和安慰剂+氟维司群组的中位PFS时间分别为16.6个月和7.2个月,与安慰剂组相比,达尔西利组可降低患者50%的疾病进展或死亡风险(单侧P < 0.0001),进一步支持该方案作为既往内分泌治疗后进展的新选择。DAWNA-2研究评估了达尔西利联合来曲唑或阿那曲唑一线治疗HR阳性、HER2阴性晚期乳腺癌的疗效和安全性,达尔西利+来曲唑/阿那曲唑组的研究者评估的中位PFS时间为30.6个月,较安慰剂+来曲唑/阿那曲唑组显著延长12.4个月,疾病进展或死亡风险降低49.0%,进一步支持该方案作为一线治疗的新选择。
5、抗Trop-2靶向治疗在乳腺癌初见成效
人滋养层细胞表面抗原2(Trop-2)是一种跨膜钙信号转导子,与肿瘤进展和预后不良有关。Trop-2在多种实体瘤中高表达,其中乳腺癌高表达比例约为78%。戈沙妥珠单抗(sacituzumab govitecan,SG)是由抗Trop2人源单克隆抗体与细胞毒性代谢物SN-38偶联而成的新型ADC,已获批适应证用于既往接受过至少二线治疗的转移性TNBC患者。
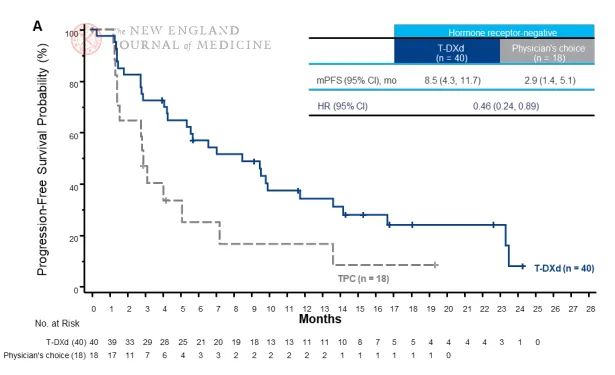
TROPiCS-02随机对照III期研究旨在探索SG在接受过内分泌治疗、CDK4/6抑制剂及二线至四线化疗的HR阳性、HER2阴性转移性乳腺癌患者中的疗效与安全性。SG与医生选择化疗相比,主要研究终点PFS时间为5.5个月和4.0个月,进展或死亡风险显著减少34%,第二次中期分析次要终点OS时间为14.4个月和11.2个月,总死亡风险显著减少21%。安全性方面,两组≥3级治疗相关不良事件发生率分别为74%和60%,SG组并未出现新的安全信号,且显著改善总体健康相关生活质量。基于此研究结果,NCCN指南推荐,既往内分泌治疗、CDK4/6抑制剂、至少二线化疗(含紫杉类)治疗进展后的HR阳性转移性乳腺癌,可考虑选择SG(ⅡA类证据)。这提示SG可为CDK4/6抑制剂耐药且多线治疗失败的HR阳性、HER2阴性晚期乳腺癌患者提供新的治疗选择。详细见:ASCO2022 | TROPiCS-02临床重磅发布:戈沙妥珠单抗使HR+/HER2-MBC进展或死亡降低34%!、J Clin Oncol:Sacituzumab govitecan治疗内分泌耐药的HR+/HER2– 晚期乳腺癌、ESMO 2022:Sacituzumab Govitecan-hziy在HER2-低表达/HER2-0转移性乳腺癌中显示出有前景的疗效(TROPiCS-02研究)
在关键的3期ASCENT研究(NCT02574455)中,SG在基线时无已知脑转移的二线或以上(2L+) mTNBC患者的主要分析人群中显示,与单药化疗医生选择治疗(TPC)相比,SG具有显著的生存优势(Bardia A et al. NEJM 2021)和生命质量(Loibl S. et al.ESMO 2021)。通过后续随访,本次展示了最终的疗效数据,包括总生存期(OS)、安全性和生活质量。
在529例入组患者中,468例基线时未发现脑转移(中位年龄:54岁[范围27-82];既往治疗线中位数:4[范围,2-17])。截至2021年2月25日(最终数据库锁定),SG (n = 235) vs TPC (n = 233)显著提高了PFS中位数(5.6 vs 1.7个月;HR:0.39;p<0.0001)和中位OS (12.1 vs 6.7个月;HR:0.48; < 0.0001)。研究组24个月时的OS率为22.4% (95% CI, 16.8-28.5), TPC组为5.2% (95% CI, 2.5-9.4)。详细见:ASCO 2022 | ASCENT临床大胜收官:面对「老大难」mTNBC,戈沙妥珠单抗实现OS/PFS双获益!
6、乐伐替尼加派姆单抗治疗晚期子宫内膜癌
在这项3期试验中,研究人员以1:1的比例将先前接受过至少一种含铂化疗方案的晚期子宫内膜癌患者随机分配接受乐伐替尼(20mg,每天口服一次)联合派姆单抗(200mg,每3周静脉内给药)或主治医师选择的化疗方案(阿霉素60mg/m2,每3周静脉内给药,或紫杉醇80mg/m2,每周静脉给药)治疗。该研究的两个主要终点是由盲法的独立审查者根据实体瘤疗效评估标准1.1版来评估的无进展生存期和总生存期。在错配修复熟练(pMMR)疾病患者和所有患者中评估终点,此外,研究人员还评估了该疗法的安全性。
该研究共纳入了827名患者(697名pMMR疾病和130名错配修复缺陷疾病),他们被随机分配接受乐伐替尼加派姆单抗(411名患者)或化疗(416名患者)。乐伐替尼加派姆单抗治疗组的中位无进展生存期比化疗组要长(pMMR人群:6.6个月 vs. 3.8个月;进展或死亡的风险比为0.60;95%置信区间[CI]为0.50至0.72;P<0.001;总体而言:7.2 vs. 3.8个月;风险比为0.56;95%CI为0.47至0.66;P<0.001)。
乐伐替尼加派姆单抗治疗组的中位总生存期比化疗组长(pMMR人群:17.4个月 vs. 12.0个月;死亡风险比为0.68;95%CI为0.56至0.84;P<0.001;总体:18.3个月 vs. 11.4个月;风险比为0.62;95%CI为0.51至0.75;P<0.001)。88.9%接受乐伐替尼联合派姆单抗治疗的患者和72.7%接受化疗的患者发生3级或更高级别的不良事件。详细见:NEJM:乐伐替尼加派姆单抗治疗晚期子宫内膜癌
7、Cemiplimab治疗复发性宫颈癌
复发性宫颈癌患者的预后往往很差。Cemiplimab是一种全人源PD-1抗体,现已获得FDA批准用于一线治疗肿瘤高表达PD-L1(TPS≥50%)、有转移性或局部晚期肿瘤、不适合手术切除或根治性放化疗、肿瘤无EGFR、ALK或ROS1畸变的非小细胞肺癌和皮肤癌。已有研究显示,Cemiplimab在复发性宫颈癌患者中有一定的抗肿瘤活性。共招募了608位患者(每组各304位)。在总试验人群中,Cemiplimab组的中位总生存期明显长于化疗组(12.0 vs 8.5个月,死亡的风险比 0.69,p<0.001)。这种生存效益在两种病理亚组(鳞状细胞癌和腺癌[包括腺鳞癌])中均保持一致。Cemiplimab组的无进展生存期也明显长于化疗组(疾病进展或死亡的风险比 0.75,p<0.001)。Cemiplimab组和化疗组的客观缓解率分别是16.4%和6.3%。Cemiplimab组PD-L1表达≥1%的患者的客观缓解率是18%,PD-L1表达<1%的患者的是11%。详细见:NEJM:采用Cemiplimab治疗复发性宫颈癌
8、二次肿瘤细胞减灭术对复发性卵巢癌患者治疗价值显现
卵巢癌患者的主要治疗方法是手术切除,随后进行卡铂和紫杉醇联合化疗。新近的研究发现,额外进行贝伐单抗或PARP抑制剂全身治疗可改善患者无进展生存。目前复发性卵巢癌的标准治疗手段为全身治疗,但仅有少数证据表明全身治疗对复发性卵巢癌患者总生存期有益。近日研究人员评估了二次肿瘤细胞减灭术对复发性卵巢癌患者的临床意义。
复发性卵巢癌患者参与研究,患者接受不含铂类化疗至少6个月后首次复发,随机接受二次细胞减灭术(手术组)或对照(单纯铂化疗),随后接受铂类化疗。患者的AGO评分阳性,ECOG评分为0,腹水少于500mL,并且在首次手术时可见病灶完全切除。研究的主要终点是总生存率,同时评估了生存质量和预后因素。
407名患者参与研究,其中206名患者接受细胞减灭术联合化疗,201名患者接受单纯化疗。手术组75.5%的患者实现了完全切除。手术组的中位总生存期为53.7个月,非手术组为46.0个月(死亡风险比为0.75)。实现完全切除患者的预后最好,中位总生存期为61.9个月。所有亚组分析中手术均更具优势。两组随访1年后的生活质量指标无显著差异,未发生术后30天内围手术期死亡事件。
研究认为,对于复发性卵巢癌患者,相比于单纯化疗,细胞减灭术后化疗可显著延长患者总生存期。详细见:NEJM:细胞减灭术后化疗可显著改善复发性卵巢癌患者预后
另一项荟萃分析也证实了这个结论,见:J Clin Oncol:二次细胞减灭术对铂敏感的复发性卵巢癌患者生存期的影响
9、cT1-2N1乳腺癌初始化疗后可根据复发风险进行适应性的降级放疗
乳腺癌的初次化疗在辅助局部放疗方面存在两难选择,因为局部放疗的指南最初是基于初次手术的病理结果。该研究目的是根据预先确定的、基于共识的研究指南,评估降级局部放疗对接受初次化疗的cT1-2N1期乳腺癌患者的肿瘤学安全性。
这项前瞻性的注册研究纳入了于2011年1月1日-2015年1月1日期间转诊至荷兰17个放射肿瘤中心之一、并接受了初次化疗和乳腺级腋窝手术治疗的cT1-2N1期乳腺癌患者。研究指南包括三个局部复发风险组,并提供相应的局部放疗建议:低危组不进行胸壁放疗和区域放疗,中危组只进行局部放疗,高危组进行区域放疗。放疗包括 25 次 2 Gy 的生物等效剂量,加量或不加量。主要终点是区域复发率。研究人员假设,5年区域复发率应低于4%。
838位患者符合 5 年随访分析的条件:低危组 291位,中危组 370位,高危组 177位。所有患者的 5 年区域复发率为 2.2%。低危组 、中危组和高危组的5年区域复发率分别是2.1%、2.2%和2.3%。如果遵循研究指南,则低风险组、中风险组和高风险组的局部区域复发率分别是2.3%、1.0%和1.4%。详细见:Lancet Oncol:cT1-2N1乳腺癌初始化疗后可根据复发风险进行适应性的降级放疗
10、PARP抑制剂鲁卡帕利在卵巢癌中获进展
(1)鲁卡帕利单药维持治疗新发卵巢癌的3期临床试验结果
接受细胞减灭术并对一线铂类双药化疗有反应的III-IV期高级别卵巢癌患者被随机(4:1)分至鲁卡帕利组(600 mg,2/日)或安慰剂组。并根据化疗后和手术时的HRD状态、残留病灶进行分层。主要终点是无进展生存期。
截止2022年3月23日,共有538位患者被随机分至鲁卡帕利组(n=427)或安慰剂组(n=111)(HRD患者:185 vs 49)。鲁卡帕利组和安慰剂组总患者的无进展生存期分别是20.2个月和9.2个月(风险比[HR] 0.52,p<0.0001);HRD患者的无进展生存期分别是28.7个月和11.3个月(HR 0.47,p=0.0004);HRD阴性患者的无进展生存期分别是12.1个月和9.1个月(HR 0.65)。
在晚期卵巢癌患者中,无论有无同源重组修复缺陷,鲁卡帕利单药作为一线维持治疗的效果良好,与安慰剂相比可获得显著的生存益处。详细:J Clin Oncol:鲁卡帕利单药维持治疗新发卵巢癌的3期临床试验结果
(2)鲁卡帕利可作为BRCA1/2突变的复发性卵巢癌化疗的替代选择
目前比较PARP抑制剂与化疗在BRCA1或BRCA2突变的卵巢癌中的疗效的前瞻性研究较少。本研究旨在评估PARP抑制剂鲁卡帕利对比以铂为基础的和非铂类为基础的化疗在BRCA1/2突变的卵巢癌中的疗效。
这是一项在多个国家的64家医院和癌症中心开展的开放标签的随机对照的3期研究(ARIEL4),招募了年满18岁的既往至少进行过2次化疗的携带BRCA1或BRCA2突变的卵巢癌患者。受试患者被随机(2:1)分成了两组,接受口服鲁卡帕利(600 mg,2/日)或化疗。主要终点是无进展生存期。
在疗效分析人群(鲁卡帕利组 220位,化疗组 105位)中,鲁卡帕利组和化疗组的中位无进展生存期分别是7.4个月和5.7个月(HR 0.64, p=0.0010)。在意向治疗人群(鲁卡帕利组 233位,化疗组 116位)中,鲁卡帕利组和化疗组的中位无进展生存期分别是7.4个月和5.7个月(HR 0.67, p=0.0017)。详细见:Lancet Oncol:鲁卡帕利可作为BRCA1/2突变的复发性卵巢癌化疗的替代选择